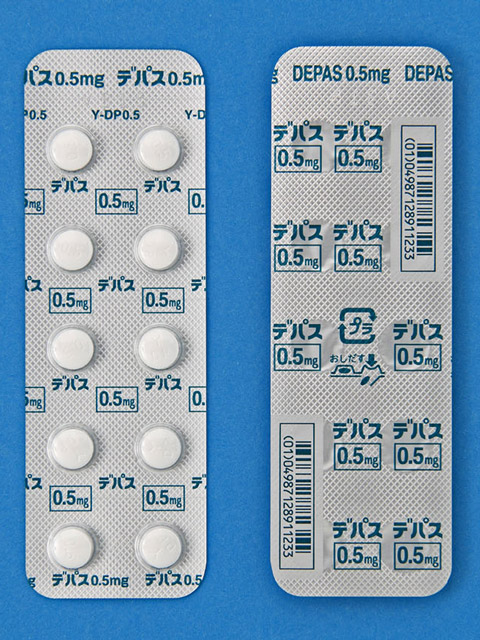
このページでは、【デパス錠】のインタビューフォームをもとに、概要と薬の名前を整理したいと思います。
これらの情報を活用する際には、必ず元の文献を確認してください。
【出典】医薬品インタビューフォーム デパス錠 改訂第18版
コンテンツ
販売名
和名
デパス錠 0.25mg
デパス錠 0.5mg
デパス錠 1mg
デパス細粒 1%
洋名
DEPAS TABLETS
DEPAS FINE GRANULES 1%
名前の由来
病的状態から)離れ= De 通り過ぎる= Pas
一般名
エチゾラム
概要
開発の経緯
デパス(一般名:エチゾラム)は,当社研究所における一連のチエノジアゼピン系化合物に関する研究により,“心身安定剤リーゼ”についで創製された精神安定剤である。
チエノジアゼピン環にトリアゾール環を縮合したデパスは,全般に薬理活性の強化が認められ,強力な抗不安作用とともに優れた鎮静・催眠作用,抗うつ作用,筋緊張緩解作用を示す。
1971年よりエチゾラム製剤の前臨床試験を開始し,その後の臨床試験により本剤の有効性,安全性並びに有用性が確認され,1983年9月に承認を取得し発売するに至った(錠0.5mg・1mg,細粒1%)。
発売後,10,720例の使用成績調査を実施し,1989年12月に再審査申請を行った。
その結果,1992年6月に「製造(輸入)承認事項の一部を変更すれば薬事法第14条第2項各号のいずれにも該当しない」旨再審査結果通知され(1992年6月3日付厚生省薬務局長通知),効能・効果及び用法・用量の表現を改めた。
また,細粒剤は2002年2月に販売名変更に伴う再承認を受け,2002年7月に変更銘柄名で薬価収載された。
さらに,医療現場では,エチゾラム製剤が処方される患者のうち,50%以上を65歳以上の高齢者が占めており,1日投与量では0.5mg/dayが最も多くなっているが,高齢者には0.5mg錠では効果が強すぎるため,さらなる低用量製剤が望まれていた。
この要望に応えるため,0.25mg錠の開発に着手し,加速試験,生物学的同等性試験を実施して2012年2月に承認を取得,2012年7月に販売を開始した。
特性と有用性
- 神経症における不安・緊張・抑うつ・神経衰弱症状に対して改善効果を示す。
- うつ病における不安・緊張に対して改善効果を示す。
- 心身症(高血圧症,胃・十二指腸潰瘍)における身体症候並びに不安・緊張・抑うつに対して改善効果を示す。
- 頸椎症,腰痛症,筋収縮性頭痛における不安・緊張・抑うつ及び筋緊張に対して改善効果を示す。
- 神経症,うつ病,心身症(高血圧症,胃・十二指腸潰瘍),統合失調症における睡眠障害に対して改善効果を示す。
- 総症例数12,328例中866例(7.02%)1,133件の副作用が報告されている。
主な副作用は、
眠気444件(3.60%)
ふらつき241件(1.95%)
倦怠感77件(0.62%)
脱力感46件(0.37%) 等であった。
(再審査終了時)重大な副作用として,
依存性,呼吸抑制,炭酸ガスナルコーシス,悪性症候群,横紋筋融解症,間質性肺炎,肝機能障害,黄疸があらわれることがある。